Arthrose du chat
L’arthrose est une maladie pluritissulaire chronique dégradative et inflammatoire, atteignant les chats avec une forte prévalence : 90% des chats de plus de 12 ans présentent des lésions radiologiques d’arthrose et 45% d’entre eux ont une expression clinique douloureuse (1).
Le cartilage mais aussi l’os sous-chondral et la membrane synoviale adoptent précocement un phénotype pro-dégradatif (consécutif à des sur-sollicitations articulaires) et un phénotype pro-inflammatoire (consécutif à des stress biologiques cytokiniques). Ainsi le cartilage ne s’use pas isolément selon une logique linéaire mais se dégrade par poussées suite à l’action d’enzymes protéolytiques et de médiateurs inflammatoires.
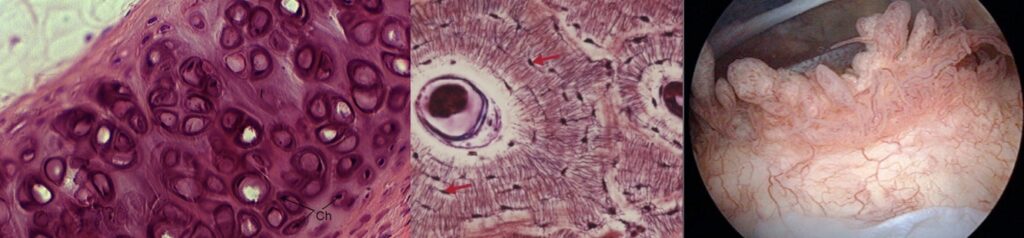
L’implication sous-jacente du système immunitaire inné humoral (via le recrutement des macrophages synoviaux et la synthèse de cytokines IL-1 et TNF) précède une inflammation chronique de faible intensité, justifiant l’appellation anglo-saxonne de « osteoarthritis ».
Cette vision pluritissulaire de la physiopathologie de l’arthrose, issue directement des données fondamentales et des études d’imagerie (IRM), pourrait aboutir dans un futur proche à des traitements personnalisés selon les atteintes tissulaires cartilagineuses, sous-chondrales ou synoviales prépondérantes (2).
Les douleurs arthrosiques ont pour origine le compartiment articulaire :
1° douleurs mécaniques s’exacerbant à l’exercice
2° douleurs inflammatoires présentes au repos, nocturnes, diminuant à l’exercice
3° douleurs neuropathiques spontanées de type « décharges électriques » accompagnées de paresthésies et de dysesthésies et le compartiment central :
4° douleurs nociplastiques : hyperalgésie et allodynie.
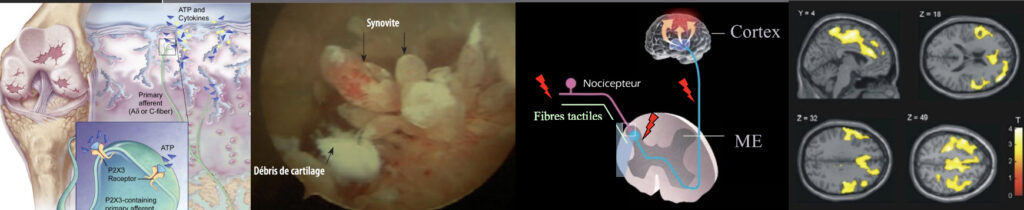
Les douleurs arthrosiques deviennent chroniques, c’est-à-dire définies comme persistantes ou récurrentes, induisant une détérioration fonctionnelle et des perturbations émotionnelles venant altérer significativement le comportement et la qualité de vie de l’animal.
Les douleurs arthrosiques évoluent en fonction de très nombreux paramètres : progression de la maladie, sensibilité inter-individuelle, conditions environnementales (climat, mode de vie, relation propriétaire–animal), nutrition, exercice, efficacité thérapeutique…
Chez le chat, les atteintes pluri-articulaires dominent
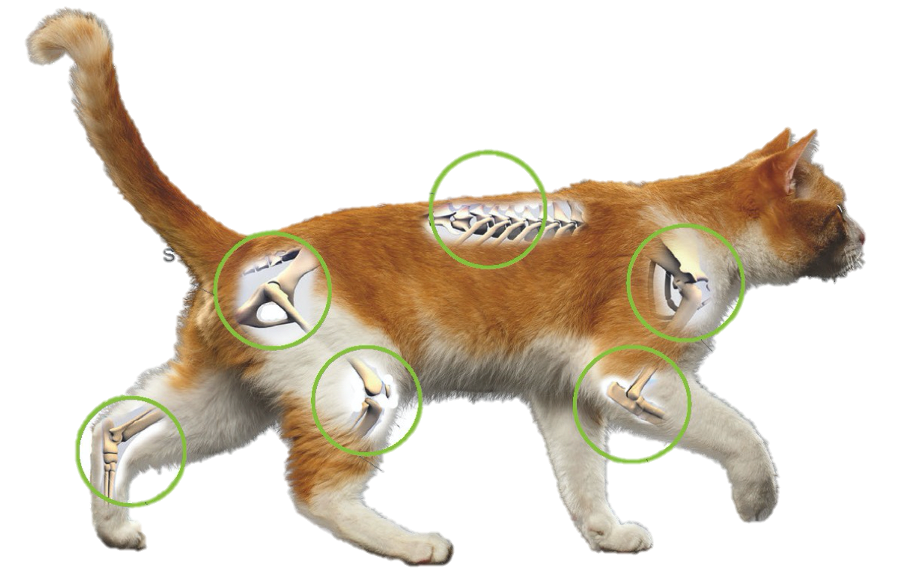
Les douleurs arthrosiques doivent être recherchées selon le déroulé suivant :
1° Médecine narrative
Le temps d’écoute donné au propriétaire est particulièrement pertinent pour rechercher les caractéristiques propres à chaque animal douloureux
Les signes décrits sont d’ordre fonctionnel :
Six critères clés ont été récemment identifiés comme très sensibles et très spécifiques des douleurs arthrosiques : Aptitude à sauter normalement en hauteur ou pour descendre, aptitude à monter ou descendre les escaliers, aptitude à courir, jouer ou maintenir une activité de prédation (3).
Les boiteries ne sont pas considérées comme des signes suffisamment évocateurs : moins de 17% des chats arthrosiques boitent en raison d’une atteinte pluriarticulaire préferentielle et de facultés adaptatives musculaires et posturales avantageuses (4) (5).
Les signes décrits révèlent parfois la qualité de la douleur : décharges électriques, hyperalgésie, allodynie, hyperpathie, activités substitutives …
Les signes décrits traduisent parfois des perturbations émotionnelles à l’origine de changements comportementaux : anxiété, états dépressifs, irritabilité, agressivité, dyssomnies, altérations des relations sociales.

2° Grilles multiparamétriques
Certaines grilles multiparamétriques comme la FMPI (Feline Musculoskeletal Pain Index) ont été développées et validées : toutefois elles ne sont pas utilisées par les vétérinaires praticiens et ont l’inconvénient d’imposer une liste fastidieuse d’items trop orientés sur la composante fonctionnelle de la douleur et souvent éloignés de la qualité de la douleur et de ses composantes émotionnelles et comportementales.
Les CSOM (Client Specific Outcome Measures) répondent aux spécificités individuelles des douleurs chroniques et cumulent des avantages décisifs :
- Renforcement de l’image du chat douloureux qui a ses propres douleurs
- Utilisation possible hors champ d’application des douleurs arthrosiques : CGSF, douleurs cancéreuses ou viscérales …
- Appropriation par les détenteurs de chats
- Remplissage aisé, archivage et interprétation dans le cadre d’un suivi à long terme grâce à la numérisation de cet outil
- Outil remarquable d’observance et d’alliance thérapeutique
3° Examen clinique et évaluation radiologique
L’examen orthopédique du chat est certes de réalisation plus difficile que celui mené chez le chien mais une procédure codifiée précautionneuse est très souvent révélatrice de dysfonctionnements pluriarticulaires.
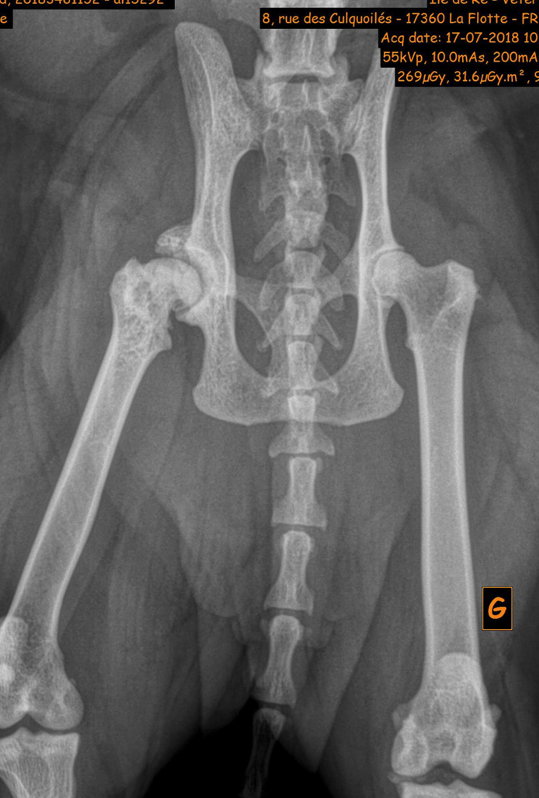
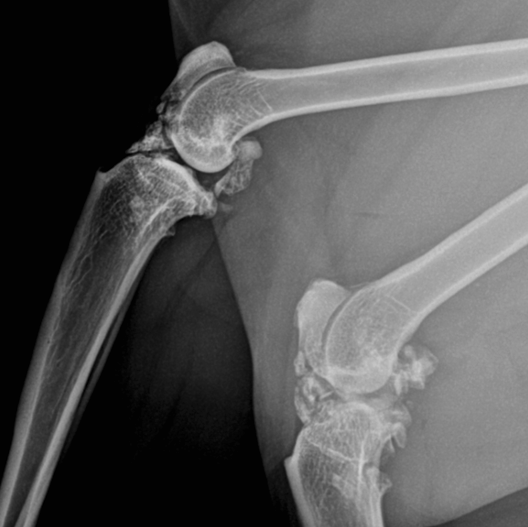
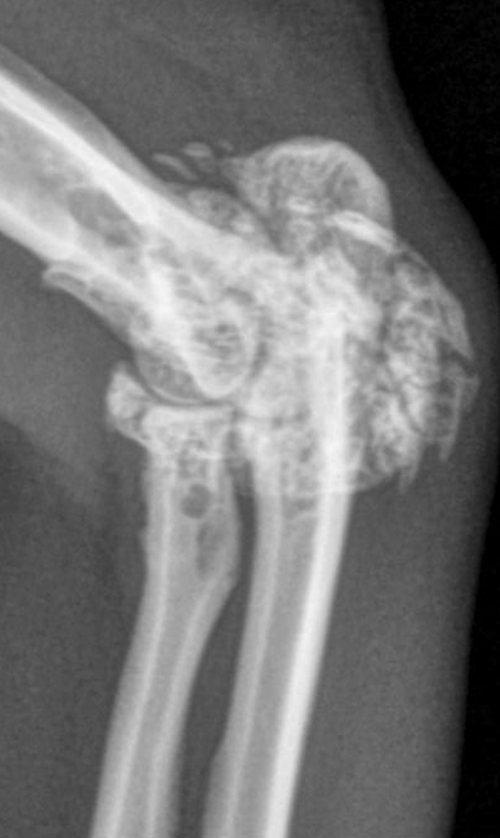
Les changements structuraux sont visibles en imagerie articulaire (prépondérance chez le chat de la minéralisation des tissus mous péri-articulaires, des ossifications synoviales, intra ou extra-capsulaires) sans qu’il y ait pour autant une corrélation exacte entre la sévérité des réactions ou des lésions et le ressenti douloureux de l’animal.
4° Outils connectés et téléconsultation
Les douleurs arthrosiques sont à l’origine d’une diminution de l’activité physique par gêne et inconfort fonctionnel, en raison des contraintes mécaniques et des nombreux stimuli nociceptifs que l’animal arthrosique perçoit. La dépression associée réduit l’envie de mobilité, tandis que les troubles du sommeil perturbent le repos nocturne en raison de l’inconfort de la position, mais aussi de l’abaissement du seuil douloureux.
Les composantes fonctionnelles et émotionnelles de la douleur peuvent être mesurées objectivement par l’accélérométrie et plusieurs études ont démontrés clairement une baisse d’activité chez les chats arthrosiques (6). Les objets connectés proposés actuellement en France n’offrent pas suffisamment de services et de garanties pour évaluer les douleurs chroniques : manque d’autonomie, taille et poids des dispositifs, pertinence des algorithmes, synchronisation des données, absence d’interface dédiée aux professionnels de santé, problème d’intégration aux logiciels métier…
La téléconsultation (dont la solution Linkyvet) dans le prolongement d’une consultation en présentiel présente l’avantage d’évaluer la douleur dans l’environnement familier du chat douloureux, loin du stress occasionné par le déplacement et la visite chez le vétérinaire ; cette téléconsultation permet aussi l’évaluation du mode de vie et oriente déjà le praticien vers des conseils personnalisés d’ergothérapie et d’amélioration de l’environnement (escaliers d’accès, panier refuge, enrichissement progressif et rassurant du milieu …)
Le projet thérapeutique individualisé des douleurs arthrosiques
oblige à la complémentarité des moyens médicamenteux, des biothérapies
et des méthodes non pharmacologiques.
L’évaluation des rapports bénéfices/risques doit toujours se faire dans la lignée de l’Evidence Based Medicine (EBM) sans oublier que celle-ci correspond à une démarche systématique associant à la formulation de la question clinique, une recherche de l’information pertinente, sa lecture critique et, enfin, son applicabilité à un patient donné avec son histoire douloureuse et ses comorbidités.
Dans ce domaine aussi subjectif de la douleur, l’EBM sera utilement complétée par de larges études cliniques observationnelles de terrain, proches de la réalité que vivent dans leur quotidien les praticiens.
En effet la grande spécificité des douleurs arthrosiques du chat est la multimorbidité traduite par les données suivantes :
Près de 70 % des chats arthrosiques souffrent de maladie rénale chronique ; 14% des chats arthrosiques seraient obèses ; de nombreux chats arthrosiques montrent parallèlement à leur expression douloureuse des signes d’hyperthyroïdie, d’hypertension et de syndrome de dysfonctionnement cognitif. La similitude des symptômes observés, notamment les vocalises nocturnes, la malpropreté, l’irritabilité et les dyssomnies doit engager le praticien dans une démarche transversale mêlant les disciplines de l’endocrinologie, du comportement et de l’algologie, car les interactions entre douleur, émotions et cognition évoluent dans des modèles circulaires auto-aggravants (7) (8) (9).
1° Approche pharmacologique
Les AINS sont prescrits pour la prise en charge des douleurs mécaniques et inflammatoires de palier I : le meloxicam augmente les pics de force verticale, la mobilité et l’activité mais ne corrige pas la sensibilisation sensorielle (6) (10).
Le tramadol est un agoniste opioïde faible et un IRSN dont cette double action a été démontrée au cours de plusieurs études cliniques. Le tramadol augmente les pics de force verticale chez le chat, améliore ou non l’activité en fonction de la dose utilisée (risque de sédation) et corrige la sensibilisation sensorielle (10).
La méthadone, opioïde fort, est utilisée en perfusion à débit constant pour la prise en charge des accès douloureux paroxystiques de palier III.
Son action anti NMDA est utilement complétée par des perfusions de kétamine au cours de la chronicisation de la douleur marquée cliniquement par des états de grande vulnérabilité (hyperalgésie, allodynie, forte comorbidité émotionnelle).
La gabapentine est prescrite en traitement de 1ère intention lors de suspicion de douleurs neuropathiques. En cas d’échec, elle peut être associée à un antidépresseur tricyclique (clomipramine) ou au tramadol ou, sous réserves d’études complémentaires, de cannabidiol.
L’action antihyperalgésique du tramadol a été démontrée par l’étude de tests sensoriels quantitatifs (11).
2° Approche non pharmacologique
Peu de compléments alimentaires ont montré une efficacité prouvée selon les critères EBM à l’exception des omégas 3 et du collagène non dénaturé de type II (12) (13).
La nutrition clinique permet de corriger les excès de poids très préjudiciables sur le plan clinique mais aussi de remédier aux fontes musculaires qui accompagnent les affections sources de fuite protéique (insuffisance rénale, hyperthyroïdie).
La physiothérapie manuelle (massages) peut être conseillée au cours d’ateliers éducatifs dispensés dans nos établissements de soins vétérinaires. La thérapie laser grâce à ses ondes du proche infrarouge offre des propriétés antalgiques, anti-inflammatoires et décontracturantes : les séances laser sont particulièrement bien tolérées par les chats arthrosiques. L’utilisation de tapis de marche voire de bassins d’hydrothérapie est parfois envisageable dans les centres spécialisés de physiothérapie.
L’ergothérapie permet de restaurer ou de maintenir des activités de manière sécurisée, autonome et efficace : il s’agit de diminuer les situations de handicap en tenant compte des habitudes de vie des animaux et de leur environnement. Différents aménagements déjà cités sont possibles ainsi que la prescription d’orthèses, à visée de stabilisation et de sécurisation des articulations.
3° Biothérapies
Les biothérapies relèvent de la production de médicaments ou de stratégies thérapeutiques basés sur le vivant. Les thérapies cellulaires intra-articulaires à base de plasma riche en plaquettes ou de cellules souches mésenchymateuses sont relativement peu utilisées chez le chat en raison de la grande prévalence des atteintes pluriarticulaires et de manque de données .
Les anticorps monoclonaux pourraient constituer une véritable révolution thérapeutique en relation avec leurs particularités pharmacocinétiques et pharmacodynamiques : Leur remarquable efficacité est liée à la pertinence de la cible, le NGF (nerve growth factor), neurotrophine indispensable à la différenciation des petites fibres C de la douleur et des fibres du système sympathique mais redoutablement impliquée dans les douleurs inflammatoires ostéo-articulaires`. Leur remarquable innocuité est liée à la spécificité de cette relation antigène – anticorps, échappant aux voies classiques du métabolisme hépato-rénal des médicaments de plus faible poids moléculaire. Le mode d’administration (une injection sous-cutanée de fréquence mensuelle) est un atout supplémentaire en faveur d’une observance améliorée (14).
Cette triple approche thérapeutique répond à la diversité qualitative des douleurs arthrosiques et s’adapte à une intensité douloureuse variable sous la dépendance de facteurs individuels fonctionnels, émotionnels et cognitifs mais aussi environnementaux.
Repenser la relation avec le propriétaire d’animal atteint d’une affection douloureuse chronique est indispensable : le maître doit être associé dès la première étape évaluative pour faciliter la compréhension des douleurs de son animal, pour partager des objectifs réalistes communs et pour la codécision du projet thérapeutique. Donner au propriétaire des compétences évaluatives et de soins entre dans le champ de l’éducation thérapeutique, complément indissociable de l’alliance thérapeutique et source motivationnelle d’une observance réussie.
1: Enomoto M et al. Anti-nerve growth factor monoclonal antibodies for the control of pain in dogs and cats. Vet Rec. 2018.
2 : Sellam J.. Bull. Acad. Natle Méd., 2018, 202, nos 1-2, 139-152, séance du 27 février 2018
3: Enomoto M et al. Development of a checklist for the detection of degenerative joint disease-associated pain in cats, J. Feline Med. Surg., 2020 Mar 3
4: Clarke S. P. et Bennett D. Feline osteoarthritis : a prospective study pf 28 cases. J. Small. Anim. Pract. 2006;47 (8):439-45.
5: Guillot M et al. Coxofemoral joint kinematics using video fluoroscopic images of treadmill-walking cats: development of a technique to assess osteoarthritis-associated disability. June 2014 Journal of Feline Medicine & Surgery 17(2)
6: Guillot M et al. Characterization of osteoarthritis in cats and meloxicam efficacy using objective chronic pain evaluation tools.
Vet J. 2013 Jun;196(3):360-7.
7: Scarlett, Janet M. and Suzanne Donoghue. “Associations between body condition and disease in cats.” Journal of the American Veterinary Medical Association 212 11 (1998): 1725-31 .
8: Marino CL et al. Prevalence and classification of chronic kidney disease in cats randomly selected from four age groups and in cats recruited for degenerative joint disease studies. J Feline Med Surg 2014 Jun;16(6):465-72.
9: Maniaki E et al., « Associations between early neutering, obesity, outdoor access, trauma and feline degenerative joint disease », J. Feline Med. Surg., 2021.
10: Monteiro BP et al. 2016 Analgesic efficacy of an oral transmucosal spray formulation of meloxicam alone or in combination with tramadol in cats with naturally occurring osteoarthritis.
11: Klinck MP et al. 2017 : Refinement of the Montreal Instrument for Cat Arthritis Testing, for Use by Veterinarians: detection of naturally occurring osteoarthritis in laboratory cats
12: Vandeweerd JM et al. Systematic Review of Efficacy of Nutraceuticals to Alleviatey Clinical Signs of Osteoarthritis. J Vet Intern Med 2012;26:448–456
13: Gencoglu H et al. Undenatured Type II Collagen (UC-II) in Joint Health and Disease: A Review on the Current Knowledge of Companion Animals. Animals 2020, 10, 697
14: Gruen M et al. A Feline-Specific Anti-Nerve Growth Factor Antibody Improves Mobility in Cats with Degenerative Joint Disease–Associated Pain: A Pilot Proof of Concept Study. J Vet Intern Med 2016







