Douleurs, émotions et changements de comportements
1° Définitions
Selon la dernière définition de l’IASP (actualisée en 2020), la douleur est :
« Une expérience sensorielle et émotionnelle désagréable associée ou ressemblant à celle associée à une lésion tissulaire réelle ou potentielle ».
Parmi les 6 notes clés complétant cette définition, il est précisé que l’incapacité à communiquer verbalement n’exclut pas la possibilité qu’un être humain ou un animal non humain éprouve de la douleur et que celle-ci peut avoir des effets négatifs sur les capacités fonctionnelles et le bien-être.
Chez les animaux de compagnie l’expression clinique de la douleur est parfois traduite par des plaintes (douleurs neuropathiques) mais le plus souvent elle relève de signes fonctionnels et/ou de changements comportementaux en relation avec le mal-être des douleurs chroniques.
Les praticiens vétérinaires rompus à l’exercice de l’hétéro-évaluation savent conjuguer une triple approche fonctionnelle, qualitative et émotionnelle de la douleur.
Le bien fondé de cette démarche repose sur la nature multidimensionnelle de la douleur dont les 4 composantes sont associées à différentes régions cérébrales interconnectées (1).
Ce modèle multidimensionnel confère un rôle dynamique à une matrice cérébrale qui se substitue à un centre unique de la douleur et qui module la perception de la douleur via les émotions et la cognition.
- La composante sensori-discriminative née de la transformation d’un stimulus thermique, mécanique ou chimique en signal électrique emprunte une voie rapide localisée (fibres A) pour être traitée au niveau des noyaux latéraux du thamalus en association avec le domaine somato-sensoriel cortical SI et SII. Elle renseigne sur le lieu, la durée, la qualité et l’intensité de la douleur (décodage du message sensoriel).
- La composante émotionnelle emprunte une voie lente, diffuse, tardive (fibres C) pour être traitée au niveau du thalamus médian, des noyaux réticulaires associés aux structures limbiques, du cortex cingulé antérieur et de l’insula. Elle confère à la douleur un caractère plus ou moins désagréable, pénible et supportable, variable d’un individu à l’autre. Lors de chronicisation, l’évolution vers l’anxiété ou la dépression est de règle. Située au coeur du cerveau , la composante émotionnelle se traduit par des réponses neurovégétatives et motrices conditionnées qui impactent les comportements.
- La composante comportementale, de même localisation neuro-anatomique, est représentée par l’expression orale (vocalises, gémissements), motrice (mobilité, jeux, sauts, dynamisme), relationnelle (dont l’agressivité) et par le retentissement végétatif.
- La composante cognitive, apanage du cortex préfrontal des Mammifères supérieurs, participe à la construction de l’image de la douleur (parfois éloignée de la réalité fidèle des lésions tissulaires), projette l’individu douloureux dans l’avenir et l’interroge sur ses rapports avec sa souffrance. Les contrôles descendants corticofuges peuvent être très efficaces (analgésie du sportif, du guerrier, hypnose…) ou au contraire déficitaires (douleurs dysfonctionnelles des fibromyalgies, des céphalées, du colon irritable…)
Le lien entre douleur et émotions est donc avéré et il doit être expliqué simplement aux propriétaires pour améliorer la pertinence de leur évaluation.
La 1ère étape est de choisir une définition compréhensible des émotions :
Les émotions (du latin ”ex-movere” qui signifie mouvement vers l’extérieur) sont des états affectifs intenses et fugaces, à valence positive ou négative, en réponse à la perception par les 5 sens d’un événement déclencheur appétitif ou aversif.
- Un évènement appétitif procure de la joie ou parfois de la surprise.
- La suppression de cet évènement appétitif entraine de la colère
ou de la tristesse. - Un évènement aversif procure de la peur ou du dégoût.
Ces 6 émotions primaires et universelles de Darwin sont instinctives et innées:
Elles apportent une réponse adaptative favorisant la survie de l’individu et de l’espèce.
Elles décernent une qualité hédonique à valeur positive (agréable, non menaçante) ou une qualité sombre à valence négative (désagréable, menaçante), à l’origine de 4 réponses :
- Réponse physiologique traduite par l’augmentation des taux de noradrénaline (médullo-surrénales) et des minéralo et glucocorticoïdes (corticosurrénales).
- Réponse musculaire et motrice objectivée par les expressions faciales, les postures, les mouvements …
- Réponse comportementale menant à des actions d’évitement (peur), de repli (tristesse) ou d’agression (colère)
- Réponse subjective mentale exprimée par ce que l’individu ressent (sentiment) et donc moins accessible à l’évaluateur ; la réalité de cette réponse subjective chez les animaux ne rencontre pas de consensus mais plusieurs études suggèrent l’existence de certaines formes de ressenti moins complexes que chez l’humain.
2° Émotions et changements comportementaux induits par la douleur
La 2ème étape est de s’interroger sur les émotions et changements comportementaux induits par la douleur au sein d’une relation réciproque : les émotions négatives tendent à augmenter la perception de douleur alors que les émotions positives la diminuent (2) (3).
Au risque d’une simplification excessive, toutes stimulations nociceptives sont à l’origine de 3 émotions négatives : la peur , la tristesse et la colère (4) (5).
Cette coloration émotionnelle est mémorisée dans le proche hippocampe et conduit à des motivations comportementales fondées sur l’apprentissage.
Lorsque ces émotions négatives sont ignorées ou prolongées, elles se transforment en émotions secondaires ou évoluent vers des perturbations comportementales (6).
- 1° La peur (état émotionnel fugace d’alarme et d’agitation déclenché par un danger spécifique et identifié, présent ou menaçant) provoque la fuite (flight), parfois l’immobilité (freeze) et a pour fonction la protection. La peur liée à la douleur aigue est adaptative puisqu’elle focalise l’attention sur la lésion et suspend les activités habituelles afin de faciliter le processus de guérison. Chez l’humain, au cours d’une douleur prolongée, la peur se manifeste par de l’hypervigilance et des attitudes d’évitement exagérées, à l’origine de comportements inadaptés teintés de pessimisme ou de catastrophisme.
La peur peut évoluer vers des états d’anxiété qui sont des états émotionnels généralisés déclenchés par une menace non spécifique, non identifiée, souvent imaginaire et attendue.
L’anticipation appréhensive d’un danger s’accompagne de sentiments d’inquiétude, de détresse et de mécanismes psychophysiologiques simples tels l’hypertonie marquée de certains muscles , source de symptômes somatiques de tension et de cercle vicieux « émotion – contracture – douleur ».
L’anxiété abaisse les seuils de la douleur et participe ainsi à sa chronicisation (7).
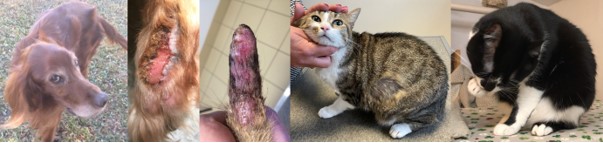
- 2° La tristesse peut évoluer vers des états dépressifs qui sont des troubles émotionnels durables en relation avec un dérèglement de l’humeur (implication des systèmes noradrénergiques, sérotoninergiques et dopaminergiques) et sources de conséquences délétères sur les activités quotidiennes. Chez les animaux de compagnie, les états dépressifs se traduisent par une asthénie, un regard triste, des refus de jeu ou de promenades, la recherche d’isolement, la perte d’interactions avec le propriétaire …
Les états dépressifs sont souvent accompagnés par des activités répétitives (plaies de léchage) puis des comportements stéréotypés: Hallucinations, polydyspsie, machonnements, ingestion de denrées non alimentaires, mordillements, sucion des flancs, tournis, aboiements compulsifs … Douleurs chroniques et états dépressifs partagent les mêmes neurotransmetteurs, des voies de communications et des structures cérébrales communes : les unes entraînant les autres dans un cercle vicieux auto-aggravant (8).
Pour autant, la prescription d’antidépresseurs ne saurait être systématique mais plutôt raisonnée : l’intérêt des AD3C est certain dans les douleurs neuropathiques mais davantage lié à un renforcement des contrôles inhibiteurs descendants qu’à un effet thymo-régulateur.

3° La colère est une émotion aversive graduelle, entre irritation et fureur.
Les aires cérébrales et les circuits neuronaux impliqués sont sous la dépendance de l’amydale et de l’hypothalamus médian.
La colère peut évoluer vers l’irritabilité puis l’agressivité (fight).
Ici les comportements d’agression sont relationnels et fondamentalement réactionnels en réponse à des situations aversives provoquées par les accès paroxystiques des douleurs neuropathiques ou inflammatoires ou par le bruit de fond constant des douleurs chroniques.

États anxieux et/ou dépressifs, irritabilité et agressivité diminuent les seuils nociceptifs et participent à l’aggravation de la douleur (modèle circulaire).
Des troubles du sommeil (dyssomnies) surviennent et la perturbation de la continuité du sommeil (et non la restriction) viennent altérer les contrôles inhibiteurs descendants. L’ensemble de ces changements comportementaux altère les relations sociales, les liens affectifs avec les propriétaires et nuisent ainsi particulièrement à la qualité de vie.
3° Évaluation de la douleur
La 3ème étape est de proposer une méthode évaluative inspirée par cette triple approche fonctionnelle, qualitative et émotionnelle de la douleur.
1° Médecine narrative
Née aux États-Unis au début des années 2000, la médecine narrative est une nouvelle approche s’inscrivant dans les soins de santé centrés sur le patient ; elle se définit comme une compétence qui permet de « reconnaître, absorber, interpréter et être ému » (Charon, 2006/2015) par les histoires de personnes malades.
Appliquée à la médecine vétérinaire, la médecine narrative devient une compétence acquise par le praticien qui sait interpréter les récits de l’histoire douloureuse de l’animal de compagnie ainsi que les circonstances de survenue des douleurs.
Grâce à la métaphore narrative, elle valorise la subjectivité à la fois de l’expérience douloureuse du propriétaire mais aussi de sa sensibilité à traduire celle de son animal.
La médecine narrative répond à la demande d’écoute du propriétaire, affiche l’empathie du praticien, amarre un 1er ancrage relationnel de confiance et devient une source dynamique de collaboration et d’adhésion thérapeutique.
Enfin elle atteste de la pertinence du modèle de l’animal douloureux présentant des douleurs spécifiques, fonction d’un bagage génétique propre, d’un vécu particulier et d’un environnement émotionnele et cognitif influent.

- 2° Les CSOM : formulation écrite des items les plus douloureux
Les Client Specific Outcome Measures s’inscrivent dans le prolongement de la médecine narrative. Ce sont des grilles évaluatives de la douleur chronique, inspirées des PRO (Patient Reported Outcome), développés en rhumatologie humaine et qui se nourrissent des symptômes ressentis et exprimés par les malades.
Appliquées en médecine vétérinaire, les CSOM font appel aux capacités d’observation d’un propriétaire partageant le quotidien de son animal pour évaluer le mal-être associé aux douleurs chroniques : handicap fonctionnel, qualité de la douleur et perturbations émotionnelles à l’origine de changements comportementaux.
La particularité réside notamment dans le fait que chaque grille est unique à l’animal douloureux. En effet, il ne s’agit pas d’un questionnaire standard mais plutôt d’un outil unique adapté à l’animal douloureux, avec son identité propre (patrimoine génétique et vécu douloureux) replacée dans son environnement émotionnel et cognitif.
Les CSOM renforcent la pertinence du projet thérapeutique multimodal, pluridisciplinaire et individualisé. Une fois les critères de douleur définis d’un commun accord entre le vétérinaire et le propriétaire, ce dernier va pouvoir lui-même effectuer les évaluations à la maison, dans l’environnement familier de l’animal.
Par le choix des 3 items les plus emblématiques de la douleur observée au cours de la dernière semaine, les CSOM formalisent la médecine narrative et autorisent le scoring et le suivi des affections douloureuses chroniques (dont l’arthrose).
Le vétérinaire échange avec le propriétaire pour définir ensemble la liste des critères à suivre.
Pour cela, l’évaluateur :
- discute de l’activité de l’animal avec le propriétaire, cherchant à lister « les activités que l’animal a des difficultés à faire ou a cessé de faire »
- recherche des qualificatifs évocateurs de douleurs mécaniques (diminuant au repos, contemporaines de l’exercice), inflammatoires (nocturnes, diminuant à l’exercice, raideur matinale), neuropathiques (spontanées, de type décharges électriques, paresthésies, dysesthésies), nociplastiques (vulnérabilité, hyperalgésie, allodynie)
- échange avec le propriétaire sur l’état émotionnel à l’origine de changements de comportement : anxiété, dépression, irritabilité, dyssomnies, altération des relations sociales.
Une fois cette 1ère liste établie, le vétérinaire demande au propriétaire de les classer par ordre d’importance pour déterminer les 3 items principaux à suivre. Le choix doit se porter sur des activités ou comportement clairement altérés, susceptibles de s’améliorer grâce à la thérapie analgésique qui sera mise en place. L’ensemble des items choisis doit refléter si possible la variété des composantes douloureuses présentes.
Une fois les items sélectionnés et précisés, les propriétaires sont invités à évaluer le degré de difficulté à effectuer ces activités ou la fréquence des modifications de comportement au cours de la dernière semaine.

Le score CSOM est l’addition des scores pour les 3 items.
Il est calculé à chaque nouvelle étape du parcours de soins de l’animal douloureux. Il permet ainsi de contrôler l’efficacité du projet thérapeutique et de suivre sur le long terme les ajustements nécessaires à la dégradation de l’affection chronique douloureuse.
La version digitale (appli) :
- Facilite le remplissage des données
- Transmet immédiatement les résultats au praticien
- Autorise l’archivage
- Visualise graphiquement l’évolution de la douleur
- Participe à l’Alliance thérapeutique
- Renforce l’expertise douleur du praticien
Découvrir l’application CAPdouleur >>>
- 3° Examen clinique
Un examen clinique attentionné, soucieux d’éviter les douleurs procédurales, complète ces deux 1ères étapes : localisation de la douleur, intensité, qualité, répercussions anatomiques (amyotrophie, ankylose …), fonctionnelles (boiterie, raideur, crépitations …), hyperalgésie, allodynie.

- 4° Parcours de suivi
La douleur est multimorphe, c’est-à-dire qu’elle se transforme tout au long de l’évolution défavorable de la maladie causale (dégénérative, inflammatoire ou proliférative) mais aussi de l’évolution heureusement favorable du projet thérapeutique.
La douleur revêt des habits tour à tour nociceptifs, inflammatoires, neuropathiques et/ou nociplastiques, sans prévisibilté particulière. Par conséquent l’évaluation doit être un processus continu et partagé entre le praticien et le propriétaire. Les visites en présentiel seront utilement complétées par des visioconsultations qui autorisent l’évaluation de la douleur dans le milieu familier de l’animal et qui permet de conseiller les meilleures stratégies de coping adaptées à l’environnement de l’animal.
La fréquence de remplissage des grilles CSOM par le propriétaire est également définie.
Prise en charge de la composante émotionnelle
Au sein d’un projet thérapeutique multidisciplinaire et individualisé, la douleur doit être prise en charge sur le plan fonctionnel mais aussi sur le plan émotionnel puisqu’une relation réciproque est présente entre douleur et émotions, ces dernières venant maintenir, aggraver ou de nouveau déclencher le processus douloureux.
1° Stratégies d’ajustement
Les stratégies d’ajustement (coping) font appel à l’ergothérapie (adapter, restaurer ou maintenir les activités) et aux améliorations de l’environnement pour diminuer les situations d’handicap fonctionnel et donc de ses répercussions émotionnelles :
Harnais, orthèses, surélévation des gamelles, tapis antidérappant, matelas à mémoire de forme, rampe ou escabeau d’accès, phéromones …
Les stratégies d’ajustement concernent aussi la régulation des émotions négatives en renforçant les liens du propriétaire avec son animal : temps consacré, nursing, massages, éducation thérapeutique (compétences évaluatives et de soins) …
2° Exercices physiques à faible impact
Les exercices physiques à faible impact en évitant la sédentarité participent au contrôle du poids, au maintien de la musculature et à prévenir l’agravation de l’ankylose. Le propriétaire mène ces exercices modérés avec sollicitude, renouant des liens de proximité avec son animal, propices à atténuer les émotions négatives.
3° Physiothérapie manuelle et instrumentale
La pratique régulière de massages par le propriétaire représente un rituel privilégié de complicité, source de relaxation musculaire et de réconfort. Les exercices de mobilisation articulaire passive (PROM : extension-flexion …) ou active (AROM : cavaletti …) sont initiés par le vétérinaire et repris par le propriétaire sous forme de jeux.
La physiothérapie laser est conseillée car en stimulant la production d’endorphines, elle réduit la peur et l’anxiété.
La physiothérapie par ondes de choc est déconseillée car elle génère une double douleur physiopathologique (ouverture des mécano et barorécepteurs) et procédurale (apréhension de l’animal) ; son action délétère sur le cartilage arthrosique (dégradation du collagène et hyperhydratation) a été récemment démontrée (9)
4° Cannabidiol
Le cannabidiol est un phyocannabinoïde issu de Cannabis sativa, dénué d’effet psychoactif (au sens récréatif du terme), contrairement au THC. Le CBD n’a pas d’affinité particulière pour les récepteurs CB1 et CB2 du système endocannabinoïde ; il est un modulateur allostérique, c’est-à-dire qu’il modifie la forme et donc le fonctionnement de ces récepteurs avec des conséquences sur l’efficacité du signal cellulaire. Le CBD agit davantage sur la composante émotionnelle de la douleur que sur la stimulation nociceptive. Les propriétés anxiolytiques (apaisantes selon le ressenti des propriétaires) seraient en relation avec l’implication du système sérotoninergique (affinité pour les récepteurs 5-HT1A, 2A, 3A).
L’effet d’inhibition de la recapture de la sérotonine et de la noradrénaline (ISRS) augmente les contrôles inhibiteurs descendants issus du tronc cérébral et participe à une analgésie généralisée et durable (10).
Une étude israélienne observationnelle de 2018 a porté sur la prise en charge de la douleur par des cannabinoïdes chez 2970 patients cancéreux. Les résultats à 6 mois montrent une amélioration significative (51%) ou modérée (45%) pour les 67% des patients ayant poursuivi le traitement ( 10% d’arrêt de traitement et 22% de décès).
La meilleure efficacité a été relevée pour l’anxiété (84%), l’agitation (88%) et l’insomnie (88%) (11).
Plusieurs études ont montré que chez l’homme les phytocannabinoïdes amélioraient la qualité et la durée du sommeil pour les les patients traités principalement pour la douleur, la maladie de Parkinson, l’apnée du sommeil, les troubles anxieux et l’état de stress post-traumatique (12) (13).
5 Psychotropes
Chez l’homme, les antidépresseurs possèdent une activité antalgique propre indépendante de leur effet thymorégulateur, liée à une inhibition de la recapture des monoamines (sérotonine et noradrénaline) au niveau des voies inhibitrices descendantes de la douleur et à un effet périphérique (blocage des récepteurs sodiques voltage-dépendants) (14).
Des arguments cliniques corroborent ces données expérimentales : analgésie obtenue à des posologies inférieures à celles nécessaires à l’effet sur l’humeur, délai d’action plus bref, efficacité également observée chez des patients douloureux non dépressifs (15).
Les antidépresseurs tricycliques (clomipramine) ont une efficacité reconnue contre les douleurs neuropathiques mais des effets indésirables histaminiques, anticholinergiques et α1 adrénergique peuvent survenir.
Des antidépresseurs plus récents (duloxétine, mirtazapine) présentent une balance bénéfices-risques plus favorables.
Les ISRS (inhibiteurs sélectifs de la recapture de la sérotonine) semblent dépourvus d’effets antalgiques (16).
Conclusion :
Les interactions entre douleurs, émotions et cognition sont complexes, interactives et très souvent auto-agravantes.
La douleur est construite par rapport à un contexte préexistant d’un vécu douloureux et en fonction d’une situation environnementale : la situation, les émotions, les attentes de l’animal, le lien avec le propriétaire, ont une influence, positive comme négative.
La prise en charge raisonnée et protectrice des douleurs chroniques doit dorénavant s’intéresser à ce triptyque en explorant davantage l’expérience construite de la douleur.
La méthode évaluative proposée (médecine narrative, CSOM, examen clinique et parcours de suivi) devrait aider à réaliser cet objectif.
La composante émotionnelle de la douleur est utilement prise en charge par des stratégies d’ajustements, la physiothérapie, probablement par le cannabidiol, éventuellement par les psychotropes après l’évaluation de la balance bénéfices / risques.
Bibliographie :
1° Calvino B. Physiologie moléculaire de la douleur. Doin. 2019
2° Morel, V., & Pickering, G. (2013). Impact de la douleur sur les processus cognitifs chez l’homme. Douleur et analgésie, 26, 11-16.
3° Estévez-López, F.; Gray,C.M., Segura-Jiménez, V., Soriano-Maldonado,A., Álvarez- Gallardo, I. C., Arrayás-Grajera, M. J., Carbonell-Baeza, A., … Pulido-Martos, M. (2015). Independent and combined association of overall physical fitness and subjective well-being with fibromyalgia severity: the al-Ándalus project. Quality of Life Research, 24(8), 1865-1873.
4° Fernandez, E., Clark, T. S., & Rudick-Davis, D. (1998). A framework for conceptualizing and assessment of affective disturbance in pain. Dans A. R. Block, E. F. Kremer, & E. Fernandez (Éds), Handbook of pain syndromes: Biopsychosocial perspectives (pp.123-147). Mahwah, NJ: Erlbaum.
5° Fernandez, E., &, Turk, D. C. (1995). The scope and signifiance of anger in the experience of chronic pain. Pain, 61, 165-175.
6° Greenberg, L. S. & Paivio, S. C. (1997). Working with emotions in psychotherapy. New York : Guilford Press.
7° Zelman, D. C., Howland, E. W., Nichols, S. N., & Cleeland, C. S. (1991) The effects of induced mood on laboratory pain. Pain, 46, 105–111.
8° Zelman, D. C., Howland, E. W., Nichols, S. N., & Cleeland, C. S. (1991) The effects of induced mood on laboratory pain. Pain, 46, 105–111.
9° Zhong Z et al. A Randomized Controlled Trial on the Effects of Low-Dose Extracorporeal Shockwave Therapy in Patients with Knee Osteoarthritis. Archives of Physical Medicine and Rehabilitation Volume 100, Issue 9, September 2019, Pages 1695-1702
10° Mello Schier et al. Cannabidiol, a Cannabis sativa constituent, as an anxiolytic drug, Rev. Bras. Psiquiatr. vol.34 supl.1 São Paulo June 2012
11° Bar-Lev Schleider L et al. Prospective analysis of safety and efficacy of medical cannabis in large unselected population of patients with cancer. Eur J Intern Med. 2018 Mar; 49:37-43.
12° Serpell, M et al. (2014). A double-blind, randomized, placebo-controlled, parallel group study of THC/CBD spray in peripheral neuropathic pain treatment. European Journal of Pain, 18(7), 999–1012
13° Blessing, E.M., M.M. Steenkamp, J. Manzanares et C.R. Marmar. « Cannabidiol as a potential treatment for anxiety disorders », Neurotherapeutics, vol. 12, n° 4, 2015, p. 825-836
14° Mico JA, Ardid D, Berrocoso E, Eschalier A. Antidepressants and pain. Trends Pharmacol Sci 2006; 27: 348-54
15° Eschalier A, Courteix C. Antidepresseurs et douleur. Rev Med Suisse 2007; 3:1581-4
16° Saarto T, Wiffen PJ. Antidepressants for neuropathic pain: A Cochrane review. J Neurol Neurosurg Psychiatry 2010;81:1372-3.






